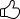본문
우리가 흔히 사용하는 건전지 AA나 AAA 이외에도 건전지의 크기에 따라 여러 유형이 있고 전지의 특성도 매우 다릅니다.
전지를 구성하는 물질이나 원리에 대해 학창시절 과학시간에 들었던 것 같긴 한데, 자세한 내용은 기억이 가물가물하죠! 오늘은 전지의 종류 및 특성에 대해 자세히 알아보겠습니다!
▣ 전지의 정의 및 구조
전지란 물질이 갖고 있는 화학에너지를 전기적 에너지로 바꾸는 장치입니다. 화학에너지에서 전기에너지로 바뀌는 과정을 방전이라고 하고 반대 과정을 충전이라고 합니다. 충전이 가능한 전지를 2차 전지라고 하고 한번만 쓰고 버리는 전지를 1차 전지라고 부릅니다.
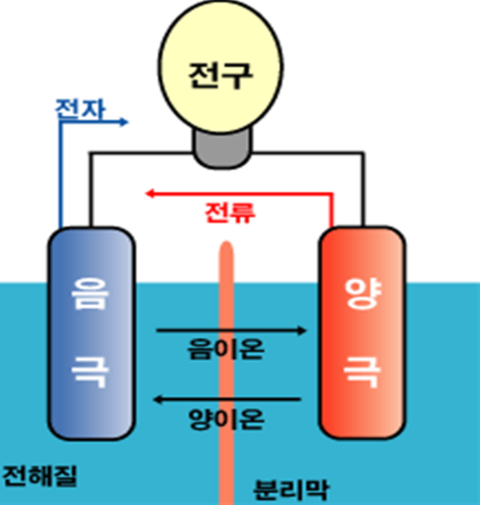
그림은 전지의 기본 원리입니다. 두 금속을 전해질용액에 넣고 도선으로 연결하면 전류가 흘러 전구에 불이 들어오게 됩니다. 두 가지 금속은 이온화 경향이 큰가, 작은가에 따라 음극이 되고 양극이 됩니다. 이온화 경향이란 전자를 잃어 이온으로 되는 정도를 나타낸 것입니다. 즉 이온화 경향이 큰 금속은 전자를 내놓고 작은 금속은 전자를 얻습니다. 이와 같이 전자를 내놓는 것을 산화이라고 하고 전자를 받는 것을 환원이라고 합니다. 그림에서 보듯이 전자는 음극에서 나와 양극으로 향하고 반대로 전류는 양극에서 나와 음극으로 들어가게 되는데요. 즉 전지는 산화, 환원반응에 의해 작동되는 장치라고 할 수 있습니다.
전해질이란 산화, 환원과정이 조화를 이루도록 이온의 이동이 일어나는 통로역할을 하는 액체 물질입니다(질산암모늄, 수산화칼륨, 질산나트륨). 분리 막은 양극과 음극이 서로 닿는 것을 방지하기 위한 차단 막입니다.산화 환원반응을 쉽게 이해하는 것은 산소를 얻거나 잃는가를 보는 것입니다. 산화는 어떤 물질이 산소와 결합하는 반응을 말합니다. 물질이 불에 타는 현상은 산화반응이 매우 빠르게 진행되는 경우이며, 금속이 부식하여 녹이 스는 과정도 산화반응입니다. 환원은 산화의 반대 개념으로 산소를 잃는 것을 의미합니다. 전자가 발견된 뒤에는 전자를 잃어버리는 현상, 수소를 잃어버리는 현상까지도 산화라고 합니다. 예를 들어 마그네슘이 염소와 반응하여 염화마그네슘이 될 때에도 산소와 반응하지 않지만 전자를 잃기 때문에 산화라 합니다. 마찬가지로 환원은 전자를 얻거나, 수소를 얻는 것입니다. 금속은 전자를 잃기 쉬운 물질로, 금속이 전자를 잃었을 때 반응이 일어난다고 합니다. 이온화 경향이란 어떤 물질이 전자를 내놓고 양이온이 되려는 성질을 말합니다. 금속은 각기 다른 이온화 경향을 갖습니다.
▣ 1차 전지 내부 구조와 용도

▣ 1차 전지의 크기별 유형별 타입
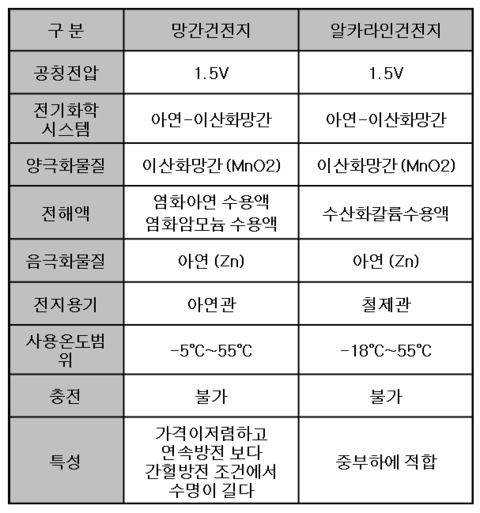
▣ 1차 전지 특성
▣ 1차 전지관련 정보
▪ 1차전지 표준품명
: 건전지, 리튬이온건전지, 망간건전지, 배터리, 버튼전지, 수은건전지, 알카라인건전지, 일회용건전지
▪ 1차전지 제조사 리스트
: (주)로케트전기, (주)벡셀, 낙원종합상사-포스렉, 한국전지, DURACELL, ENERGIZER, Golden Power, MAXWELL,PANASONIC, SANYO, SUN MIRACLE, TOSHIBA

글 / 이혜원
(won@i-db.co.kr)| 작성기사 더보기 
[ⓒ 산업정보포털 idb.imarket.co.kr, 무단 전재 및 재배포 금지]